Atendimento odontológico em grávidas
Você sabia … … Que o melhor período, durante a gravidez, para se tratar os dentes é entre o 4o e o 6o mês? … Que existe… Read More »Atendimento odontológico em grávidas
Você sabia … … Que o melhor período, durante a gravidez, para se tratar os dentes é entre o 4o e o 6o mês? … Que existe… Read More »Atendimento odontológico em grávidas
Entrevista concedida à revista da APCD (Associação Paulista dos Cirurgiões Dentistas) – São Paulo
Sem dúvida, os anestésicos locais constituem a mais importante classe de drogas para o controle da dor em Odontologia, pois são necessários em quase todos os procedimentos clínicos. São os medicamentos mais utilizados pelo cirurgião dentista, portanto, o conhecimento dos efeitos que exercem sobre o organismo, principalmente sobre o Sistema Cardiovascular e Sistema Nervoso Central e o seu desempenho no combate aos fatores estressantes dos atendimentos odontológicos, são, sem dúvida, fundamentais.
Estudos comprovam que a escolha correta do anestésico local, bem como o uso de técnicas anestésicas precisas, podem controlar a ansiedade do paciente, pois o rigor técnico associado à eficácia anestésica tornam os procedimentos odontológicos indolores e seguros. A segurança de que o paciente esteja realmente anestesiado, ou seja, a certeza da efetividade anestésica é imperiosa para o controle do estresse durante o procedimento odontológico.
O anestésico local tem a vantagem de suprimir a transmissão do impulso nervoso de forma reversível. Traz conforto ao paciente e tranquilidade ao profissional. É seguro quando usado adequadamente, na dose correta e com técnicas precisas realizadas com uma seringa de aspiração. Além da sua reversibilidade, as propriedades ideais de um anestésico local são: baixa toxicidade, eficácia quando aplicado sobre a mucosa, tempo de indução rápido, duração compatível com o procedimento, esterilidade, estabilidade e isenção de reações alérgicas.
Essas características variam de uma base anestésica para outra, mas, em geral, os anestésicos locais são drogas com baixa toxicidade. Não há relatos na literatura de alergia aos anestésicos locais do tipo amida, por exemplo.
Quando aplicados em concentrações apropriadas, os anestésicos locais deprimem de maneira reversível a condução nervosa em tecidos excitáveis, sendo, portanto utilizados nas anestesias locais e também como antiarrítmicos. Impedem a despolarização da fibra nervosa, responsável pela transmissão do impulso nervoso. Atuam por ligação aos receptores específicos dos canais de sódio (glicoproteínas). Figura 1.
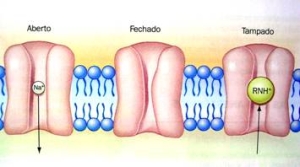
Fonte: MALAMED, S.F. Manual de Anestesia Local. Rio de Janeiro: Elsevier, 2005, p. 55-82.
A maioria dos anestésicos locais é composta por aminas terciárias. A sua estrutura é formada por uma parte lipofílica, representada pelo anel benzênico, e uma parte hidrofílica, derivada do álcool ou do ácido acético, e uma cadeia intermediária. (Figura 2).
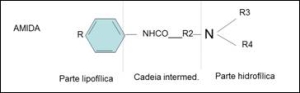
Os anestésicos locais são compostos básicos, pouco solúveis em água e instáveis quando expostos ao ar. Devido a isso são associados aos ácidos para formar sais, denominados de Cloridratos. Portanto são chamados de Cloridrato de Lidocaína, Cloridrato de Mepivacaína, Cloridrato de Articaína, Cloridrato de Prilocaina, Cloridrato de Bupivacaína, Cloridrato de Benzocaína, e assim por diante.
Quando o anestésico local é injetado no tecido, nas proximidades do nervo, para realizar efeito anestésico, ele se apresenta de forma dissociada. Ou seja, existem moléculas com carga positiva (cátions), chamadas de RNH+ e moléculas sem carga, RN (base). A fórmula da dissociação do anestésico local pode ser assim representada: RNH+ RN + H. A molécula catiônica (RNH+) é hidrofílica e responsável pela difusão do anestésico local pelos tecidos. A molécula sem carga, a base, (RN) é lipofílica e responsável pela entrada do anestésico no nervo. Quando o pH tecidual está mais alto, o equilíbrio químico é desviado para a direita: RNH+ < RN + H, ou seja, existem mais moléculas na forma de base do que moléculas catiônicas. E o inverso também ocorre, quando o pH tecidual está mais baixo, o equilíbrio químico é desviado para a esquerda: RNH+ > RN + H, existem mais moléculas catiônicas do que na forma de base. Portanto, a dissociação do anestésico local depende do pH do tecido e do pKa da solução anestésica. O pKa é o pH em que há maior dissociação do anestésico local. Em outras palavras, é o pH em que o anestésico local se apresenta com 50% de moléculas catiônicas (RNH+) e 50% de moléculas na forma de base (RN). Quanto maior o pKa do anestésico menor a porcentagem de moléculas na forma de base, e portanto, maior o tempo de indução anestésica.
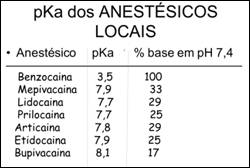
Por outro lado, quanto mais moléculas catiônicas estiverem presentes, maior será a difusão anestésica. Quanto mais moléculas na forma de base, melhor a penetração do anestésico no nervo.
Esses fatores explicam o tempo de início de ação do anestésico local. Outros fatores podem interferir na sua ação. A solubilidade em lipídeos, por exemplo, quanto maior a solubilidade em lipídeos maior a potência e a duração da anestesia. A ligação às proteínas plasmáticas também interfere positivamente na duração anestésica.
A maioria dos efeitos tóxicos de natureza grave relaciona-se a concentrações sanguíneas elevadas, atingidas por meio de injeção intravascular acidental ou pela administração de grandes quantidades da droga. Os maiores riscos para a saúde são representados pelas convulsões, depressão cardiorespiratória e colapso cardiovascular decorrentes de doses excessivas.
Em adultos saudáveis, normotensos, a dose máxima permitida de lidocaína a 2% é 300 mg, ou 8,3 tubetes. A dose máxima de prilocaína a 3% é de 420 mg, ou 7,4 tubetes. Quando o anestésico local está associado ao vasoconstritor, a dose máxima recomendada é maior porque o vasoconstritor diminui a toxicidade do anestésico local. Veja o quadro de doses máximas recomendadas de anestésicos locais, com e sem vasoconstritores, na Figura 4.
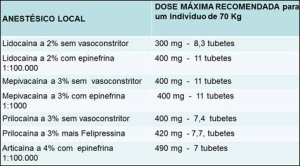
É muito importante que o cirurgião dentista conheça as doses máximas recomendadas de anestésico local, com e sem vasoconstritor, para um indivíduo adulto de 70 kg. A partir desse conhecimento, o profissional deve realizar o cálculo da dose máxima, individualizando-a para o seu paciente. Se a paciente for uma mulher de 55 Kg, por exemplo, a dose máxima de Lidocaína a 2%, individualizada para ela, passaria a ser de 236 mg, o que corresponde a 6,5 tubetes de 1,8 ml.
Em crianças a dose máxima recomendada é reduzida substancialmente. Se tomarmos como exemplo uma criança de 5 anos com 18kg, a dose máxima recomendada de lidocaína a 2%, individulizada para essa criança, é de 77 mg, o que corresponde a 2,1 tubetes de lidocaína a 2% sem vasoconstritor. Veja que é uma quantidade muito pequena de anestésico local.
A susceptibilidade individual também possui papel importante na determinação do potencial de toxidade do anestésico local. Este fato deve ser considerado durante a realização das técnicas anestésicas adequadas, com injeções lentas, e evitando-se injeções intravasculares. Uma boa anamnese, com detalhado levantamento da história médica do paciente, é primordial para que a escolha do anestésico local e do vasoconstritor seja correta.
O anestésico local é depressor do Sistema Nervoso Central, porém quando administrado em doses excessivas, as manifestações clínicas são de excitação. Isso ocorre porque o anestésico local inibe as vias inibitórias, deixando as vias excitatórias sem oposição. Vertigem, tontura, analgesia, parestesia, distúrbios áudio-visuais, apreensão e confusão mental são sinais de inibição do Sistema Nervoso Central (SNC). A superdosagem pode levar à convulsão, depressão de SNC, hipotensão profunda e colápso cardíaco.
O Sistema Cardiovascular (SCV) também pode ser afetado pelo anestésico local, que é considerado seu depressor. Ele diminui a excitabilidade elétrica do coração, a velocidade de condução e a força de contração do miocárdio, e promove a vasodilatação periférica. Devido a essas características, a lidocaína é utilizada como antiarrítimico.
Devido à sua ação vasodilatadora, o anestésico local sem vasoconstritor é absorvido mais rapidamente pelo SCV. Como consequência há uma diminuição da efetividade terapêutica no local da injeção, com aumento da concentração plasmática da droga, e por portanto, o aumento da toxicidade e do sangramento.
É importante lembrar que as drogas vasoconstritoras são incorporadas em pequenas concentrações às soluções anestésicas com a finalidade de melhorar a qualidade e duração da anestesia e, presumivelmente, de diminuir a toxidade sistêmica. São associadas aos anestésicos locais para equilibrar a sua ação vasodilatadora, diminuir o fluxo sanguíneo e a perfusão, diminuir a concentração plasmática e consequentemente a toxicidade. Em geral, os efeitos tóxicos produzidos pelos vasoconstritores ocorrem antes daqueles provenientes dos anestésicos locais, e como consequencia podem constituir um fator limitante na dose da solução anestésica. Por outro lado, a dose máxima recomendada de um anestésico local com vasoconstritor é maior do que a dose máxima de um anestésico sem vasoconstritor.
Os vasoconstritiores associados aos anestésicos locais são quimicamente idênticos aos mediadores químicos do Sistema Nervoso Simpático: adrenalina e noradrenalina, com exceção da felipressina, que é um hormônio sintético do lobo posterior da hipófise, caracterizado por propriedades vasoconstritoras. Por isso são chamadas de drogas simpatomiméticas ou adrenérgicas. Os vasoconstritores normalmente associados aos anestésicos locais são: a epinefrina (adrenalina); norepinefrina (noradrenalina); levonordefrina; fenilefrina e felipressina.
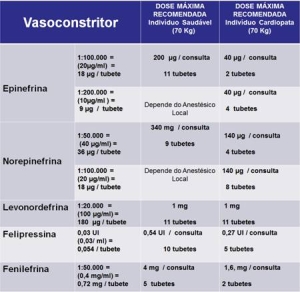
Em doses baixas, até 0,1 mg/ml, a adrenalina (epinefrina) provoca respostas beta-adrenérgicas: aumento da Frequência Cardíaca, do Volume Sistólico, da contratilidade do miocárdio, diminuição da Pressão Arterial Média e da Resistência Vascular Periférica. Possui efeito vasodilatador arteriolar e vasoconstritor local. Em doses altas, a epinefrina provoca alterações alfa-adrenérgicas: aumento da Pressão Arterial Sistólica, Diastólica e bradicardia reflexa. Veja o quadro com as doses recomendadas de vasoconstritores. Figura 5.
[/fusion_builder_column][fusion_builder_column type=”1_1″ background_position=”left top” background_color=”” border_size=”” border_color=”” border_style=”solid” spacing=”yes” background_image=”” background_repeat=”no-repeat” padding=”” margin_top=”0px” margin_bottom=”0px” class=”” id=”” animation_type=”” animation_speed=”0.3″ animation_direction=”left” hide_on_mobile=”no” center_content=”no” min_height=”none”]
A norepinefrina, independente da dose, provoca respostas alfa-adrenérgicas: aumento da Pressão Arterial Sistólica, Diastólica e Média, aumento do Débito Cardíaco, da contratilidade do miocárdio e da Frequência Cardíaca.
A levonordefrina possui as características farmacológicas semelhantes da epinefrina, porém o seu efeito vasoconstritor é 15% do efeito da epinefrina.
A Fenilefrina, devido à ação direta nos receptores alfa-adrenérgicos promove: vasoconstrição periférica; libera norepinefrina nas sinápses do SNC (ação indireta), o que leva ao aumento da resistência vascular periférica, aumento do débito cardíaco, aumento da Pressão Arterial Média e bradicardia reflexa. A fenilefrina deve ser evitada em pacientes cardiopatas e que tomam anti-hipertensivos, antiarrítimicos, betabloqueadores, e antidepressivos tricíclicos.
A Felipressina não tem ação simpatomimética. Não apresenta nenhuma resposta cardiovascular significante. Reduz o fluxo sangüíneo local por causar contração da musculatura lisa vascular. Acentua a contração uterina, por elevar o efeito da oxitocina. Portanto, está contraindicada para pacientes grávidas, e está muito bem indicada para pacientes cardiopatas, hipertensos, sob efeito de anti-hipertensivos, ou betabloqueadores.
Devemos considerar ainda que o paciente bem anestesiado apresenta menor incidência de alterações cardiovasculares, pois a ausência de dor e a tranquilidade advinda dessa condição evitam o estresse e a liberação das catecolaminas endógenas. Sabemos que a manipulação dos tecidos orais, o medo, a ansiedade, o estresse psicológico e o desconforto, associados à injeção oral, podem produzir alterações cardiovasculares não detectadas clinicamente, e muitas vezes, mais importantes do qua aquelas provocadas pela injeção intravascular acidental de anestésico local com vasoconstritor.
A atividade parassimpática com bradicardia e, ou síncope até mesmo arritmias cardíacas podem ser experimentadas durante a visita ao dentista, como conseqüência da ansiedade. Pacientes saudáveis, geralmente, são capazes de tolerar as respostas fisiológicas decorrentes do estresse, porém, pacientes hipertensos, cardíacos, com doenças cérebro-vasculares ou idosos podem ter a tolerância ao estresse diminuída.
Pacientes que recebem antidepressivos ou inibidores da mono-amino-oxidase (MAO), fármacos bloqueadores neuronais adrenérgicos (fentolamina, tolazoína, alcalóides de ergot, fentiazínicos, clorpromazina, propanolol e guanitidina), halotano e hormônios tireoideanos também devem ser considerados na seleção do anestésico local e na determinação da dosagem máxima permissível de vasoconstritores.
A escolha correta do anestésico local, bem como o uso de técnicas anestésicas precisas, podem controlar a ansiedade do paciente, pois o rigor técnico, que pode ser alcançado com o uso de seringas de aspiração para evitar a injeção intravascular acidental, associado à eficácia anestésica tornam os procedimentos odontológicos indolores e seguros. A segurança de que o paciente esteja realmente anestesiado, ou seja, a certeza da efetividade anestésica é imperiosa para o controle do estresse durante o procedimento odontológico.
Muitos pacientes ainda se incomodam com a visita ao dentista. Ficam ansiosos e consideram o procedimento odontológico um fator estressante. Os cirurgiões dentistas têm consciência de que o medo e a ansiedade podem trazer muitas alterações fisiológicas durante uma consulta. Por isso a resposta fisiológica do organismo frente aos procedimentos odontológicos de rotina vem sendo estudada e debatida por muitos autores ao longo dos anos, principalmente nos procedimentos invasivos.
Venho estudando os efeitos terapêuticos e adversos do anestésicos locais desde meu ingresso na Faculdade de Odontologia da USP, em 1989, como professora de anestesiologia. A minha Dissertação de Mestrado na FOUSP, sob o tema de “Alterações cardiocirculatórias decorrentes da injeção intravascular do Cloridrato de Lidocaína a 2 % associado ao Cloridrato de Noradrenalina (20ug/ml) em ratos acordados” resultou na publicação de artigo científico na revista Anesth Progress (2007) em parceria com meu orientador, Prof. Dr Paschoal Armonia, atual diretor do Instituto de Ciências da Saúde da UNIP e com o Professor Dr Stanlay Malamed, autor inúmeros artigos científicos, capítulos de lívros e livros de anestesiologia, como Manual de Anestesia Local (2011).
Esse trabalho avaliou os efeitos cardiocirculatórios da injeção intravascular do Cloridrato Lidocaína a 2% mais norepinefrina (1:100.000) em ratos Wistar, simulando a injeção intravascular acidental em humanos. A dose administrada foi proporcional a um cartucho de anestésico local (1,8 mL), em um ser humano de 70Kg, o que é equivalente a 0,51 mg/kg de cloridrato de lidocaína e de 0,51 µg/kg de cloridrato de norepinefrina. O tempo médio de injeção foi de 15,7 segundos. Os resultados desse estudo mostraram aumentos significativos na pressão arterial sistólica, diastólica e pressão arterial média e uma diminuição no rítmo cardíaco. A maior variação ocorreu na pressão arterial sistólica, durante a injeção do anestésico local, e no primeiro minuto após a administração da solução anestésica.(FARACO, F.N.; ARMONIA, P.L.; MALAMED, S.F. Cardiovascular alterations after injection of 2% lidocaine with norepinephrine 1:50,000 – Xylestesin – in rats. Anesth Progress, 2007 Summer; v.54, n.2, p.45 -49).
Os resultados desse estudo mostram que a injeção intravascular acidental pode provocar altrações cardiocirculatórias não detectáveis clinicamente e portanto, todo cuidado deve ser tomado para evitar a injeção endovenosa durante a anestesia. O recurso mais adequado para evitar a injeção intravascular é o uso de seringa de aspiração, associado às técnicas anestésicas precisas. Outro fator importante para o controle de efeitos indesejáveis provenientes do anestésico local é a injeção lenta, pois se alguma alteração clínica for observada, a anestesia deve ser interrompida e dessa maneira, pouco anestésico foi injetado.
É importante ressaltar que nesse trabalho a velocidade de injeção foi muito alta, foram gastos apenas 15,7 segundos. Malamed recomenda que a anestesia pterigomandibular, por exemplo, seja administrada em 2 minutos.
Os resultados desse trabalho nos alertaram para um outro fator importante que deve ser ressaltado, a escolha do vasoconstritor. A noradrenalina (ou neorepinefrina), escolhida em nosso trabalho, possui mais desvantagens do que vantagens para o uso em pacientes comprometidos cardiologicamente.
Como já disse antes, a norepinefrina, mesmo em doses baixas tem respostas alfa-adrenérgicas, ou seja, aumenta a pressão arterial, o débito cardíaco e a contratilidade do miocárdio, e a resistência vascular periférica, portanto deve ser evitada em pacientes cardiopatas. Ao contrário da adrenalina (epinefrina), que em doses baixas provoca respostas beta-adrenérgicas: aumento da Frequência Cardíaca, do Volume Sistólico, da contratilidade do miocárdio, porém promove a diminuição da Pressão Arterial Média e da Resistência Vascular Periférica. Isso quer dizer que em doses baixas, evitando-se a injeção intravascular acidental, a epinefrina, devido a sua eficácia em potencializar o efeito anestésico e em promover uma boa hemostasia, é mais segura, e pode ser indicada em pacientes cardiopatas, desde que a dose máxima recomendada seja respeitada.
A American Hearth Association recomenda que, em pacientes cardiopatas, a dose máxima de epinefrina seja de 40 µg por consulta, o que representam 2 tubetes de anestésico contendo epinefrina 1:100.000 (18µg) ou 4 tubetes de anestésico contendo epinefrina 1:200.000 (9µg/ml).
Sabendo que o medo, a ansiendade e o estresse podem provocar alterações cardiocirculatórias nem sempre detectadas pelo clínico, ou erroneamente atribuídas ao anestésico local, realizamos outros estudos quando avaliamos os efeitos do estresse na hemodinâmica cardíaca durante o atendimento odontológico.
Em um estudo duplo-cego, avaliamos as alterações cardiocirculatórias de pacientes sob o efeito de um ansiolítico, o diazepam 10 mg, ou do placebo, durante o atendimento odontológico, sob o efeito da lidocaína a 2% mais epinefrina 1:100.000. Os pacientes não receberam medicamento, ou receberam 10 mg de diazepam, ou de placebo, 1 (uma) hora antes do procedimento. Nem o paciente nem o profissional sabiam se o comprimido administrado era o placebo ou o diazepam. Os pacientes foram monitorados por um monitor automático não invasivo de pressão arterial, frequencia cardíaca e oximetria, nos períodos pré, trans e pós-operatórios. Os parâmetros cardiocirculatórios (pressão arterial sistólica, diastólica, média, a frequencia cardíaca e a oximetria) foram registradas a cada 1 minuto. Os valores dos parametros foram obtidos nas fases: 15 minutos antes da anestesia; durante a anestesia tópica, durante a anestesia; 5 minutos após a anestesia; durante o preparo cavitário; durante o procedimento restaurador; por 10 minutos após o término. Os pacientes foram divididos em 3 Grupos: A (sem pre-medicação); B (precedidos de diazepam – 10 mg) e C (precedidos de placebo). Todos receberam anestesia infiltrativa, contendo 1,8 ml de lidocaina a 2 % (36mg) mais epinefrina 1:100.000 (18µg). Não foram encontradas alterações dos parametros cardiovasculares durante os procedimentos clínicos. Quando comparados entre si, os grupos apresentaram diferenças estatisticamente significantes na pressão arterial diastólica, durante a anestesia. O grupo B (precedido de diazepam) apresentou a pressão arterial diastólica maior que o grupo C (placebo). Em outras palavras, o condicionamento do paciente, uma boa conversa, uma boa anestesia e a segurança que o profissional transmite para o paciente são tão benéficos, ou mais, que o uso de diazepam, em procedimentos de rotina.
O mesmo não pode ser afirmado para procedimentos mais invasivos, como cirurgias de implantes, por exemplo. Realizamos um outro estudo sobre estresse de pacientes que foram submetidos a cirurgias de implantes, sob o efeito do óxido nitroso.
A finalidade deste estudo foi avaliar os parâmetros cardio-circulatórios (pressão arterial sistólica, pressão arterial diastólica, pessão arterial média, freqüência cardíaca, saturação de oxigênio) e os níveis séricos de catecolaminas (epinefrina, norepinefrina e dopamina), durante a cirurgia para colocação de implantes. Dez pacientes, com idade entre 18 e 65 anos, normotensos, receberam 2 cirurgias para colocação de implantes na maxila ou mandíbula, sob efeito da mepivacaína a 3% mais norepinefrina 1:100.000, perfazendo um total de 20 cirurgias. Foram monitorados nos períodos pré, trans e pós-operatórios, por meio de monitor automático não invasivo para pressão arterial e freqüência cardíaca, (MX3-Emae-Transmae-SP-Brasil), de modo contínuo a cada 2 minutos. Os primeiros 15 minutos, durante o preparo do paciente, foram considerados como Período Basal. Os pacientes foram divididos em Grupo A (sem o uso do Óxido Nitroso e Oxigênio) e Grupo B (sob a ação do Óxido Nitroso e Oxigênio). Não foram encontradas alterações nos parâmetros cardiocirculatórios, durante as cirurgias de colocação de implantes, em ambos os grupos . Quando comparados entre si, o grupo B apresentou Freqüência Cardíaca menor e saturação de Oxigênio maior que o Grupo A. Os níveis séricos de Dopamina foram maiores no Grupo B. Não houve aumento da concentração sérica de epinefrina e norepinefrina em ambos os grupos. O uso da sedação com Óxido Nitroso e Oxigênio mostrou-se seguro, quanto aos parâmetros cardiocirculatórios, neste modelo experimental.
Read More »Anestesia odontológica